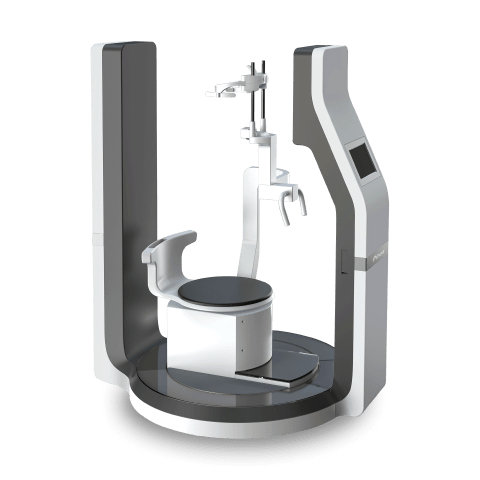
有方医疗的FDA征程:以创新为翼,普惠全球健康
2025-07-30
喜报,有方医疗获得FDA认证
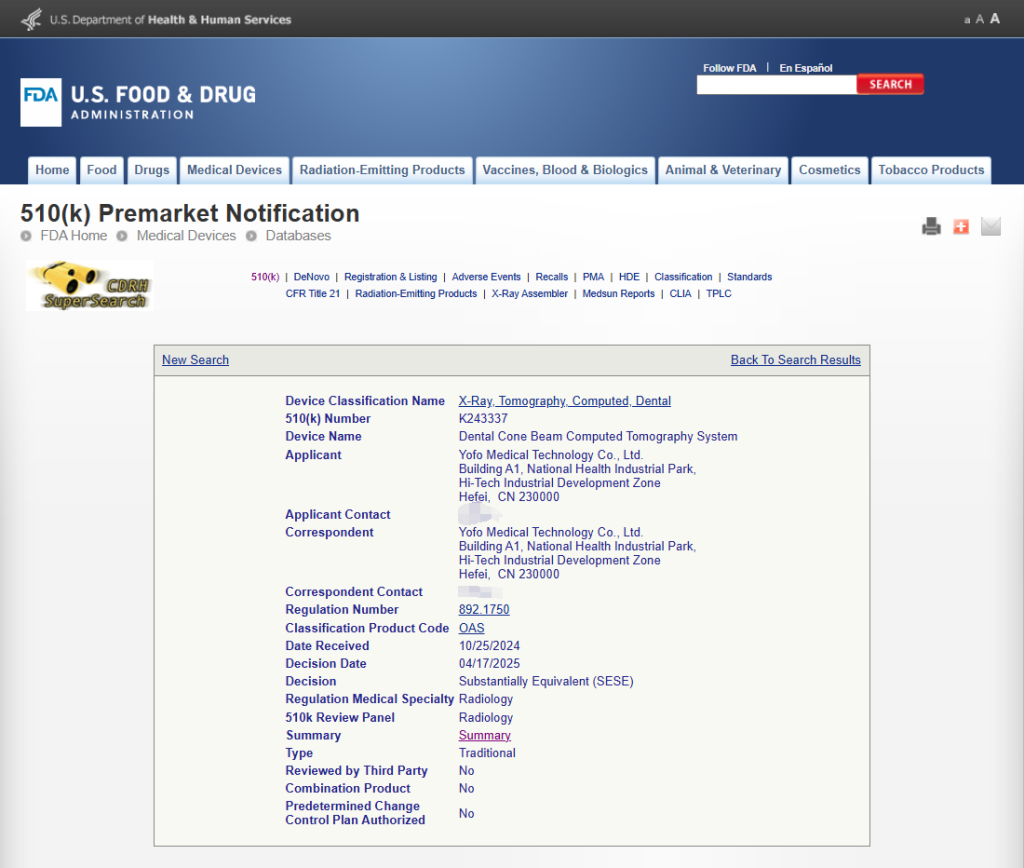
什么是FDA?
FDA,全称为美国食品药品监督管理局(U.S. Food and Drug Administration)。FDA 成立于1906年,是美国联邦政府下属的独立监管机构,负责对食品、药品、医疗器械、化妆品等产品的安全与有效性进行监管,覆盖美国本土及全球150多个国家和地区的进口医疗产品,是美国乃至全球最负盛名、最具权威的公共卫生机构。
这份认证不仅意味着有方医疗口腔CT通过了全球最严苛的监管标准,更标志着中国医疗创新力量正式叩开了国际高端市场的大门。有方医疗用十年磨一剑的坚守,书写了一段中国医疗科技企业的全球化突围之路。

派CT:坚守品质,征服FDA严苛审核
(1)派系列CT
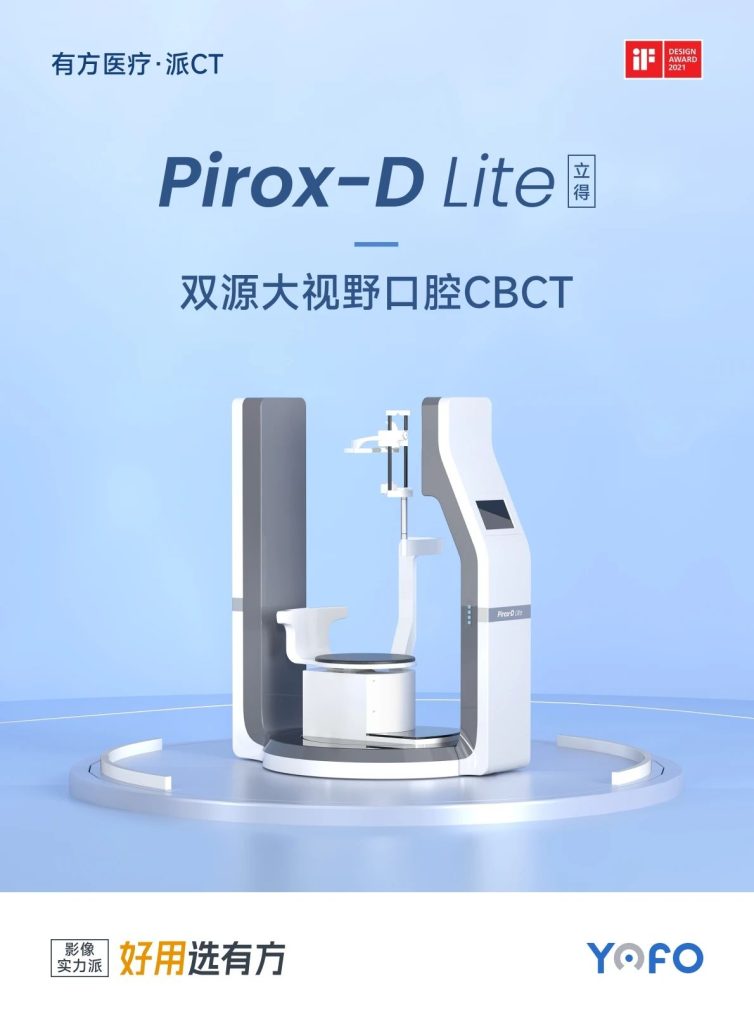
派CT,在外观上,突破传统口腔CT造型,兼顾科技与美学,采用顶部开放落地旋转坐式结构,有效减轻患者的压抑感,提升诊疗舒适度。在成像上,采用全球首创双源并行扫描技术,拍一次就可以生成CT、全景以及正侧位。最高空间分辨率可达40lp/cm,最大视野可达24*21cm。在实现高清成像和大视野的同时,还兼具超低辐射剂量的特点,仅有常规辐射剂量的四分之一,显著降低患者所受辐射风险。

(2)FDA说我们是“Novel”!全球首创双源口腔CT,凭什么这么牛?
在申请FDA认证的过程中,我们经历了一个让团队振奋的“小插曲”——原本按照口腔CBCT的常规注册路径,我们完全可以走标准的等同性申报,无需提供额外的临床影像数据。
但!因为我们有全球首创的“双源坐式”及“图像重建算法”技术,这套创新架构在国际审查中引起了FDA的高度关注。FDA在审评意见中,罕见地使用了一个评价词——“Novel”,意思是:新颖的、独特的、前所未有的。FDA在医疗器械审评中一向以“严谨”著称。能被称为“Novel”,说明我们的技术架构和使用方式,在全球范围都具备突破性和先进性。
为了回应这份认可,我们主动追加提交了临床影像数据,以更充分地展示产品在真实诊疗场景下的成像效果与使用优势。我们愿意多走一步,只为让产品的安全性与临床价值更加经得起推敲。

(3)派系列最新款“派·立得”全国发售
深远意义
获得FDA认证的这一刻,我们深知,这不仅是公司的一个里程碑,更是我们践行“坚持临床驱动,引领跨代革新,打造普惠高效的医疗器械产品,让每个人都能‘看见’自己的健康”使命的起点。这一成就不仅标志着我们在全球医疗器械市场迈出了坚实的一步,更展现了中国医疗器械企业的创新实力与国际竞争力。
这份里程碑式的认可,让我们更加坚定前行的方向。我们相信,只要坚持技术创新与临床价值并重,就能在全球医疗健康领域,发挥越来越重要的作用。